проверени факти рецензирана публикација
лекторирани
by Kimberly Hickok, Chan Zuckerberg Biohub
Инфекцијата на долниот респираторен тракт (LRTI), која вклучува состојби како пневмонија, долго време е водечка причина за смрт од заразни агенси и водечка причина за смрт кај децата ширум светот. Но, и покрај неговата распространетост, LRTI е незгодно за лекарите да го третираат ефикасно бидејќи сегашниот дијагностички пристап често не успева дефинитивно да утврди дали воопшто постои инфекција и ако е така, кој патоген ја предизвикува.
Сега, во една студија објавена во The Journal of Clinical Investigation, тим предводен од истражувачи од Chan Zuckerberg Biohub San Francisco (CZ Biohub SF), UC San Francisco (UCSF), Медицинскиот кампус на Универзитетот во Колорадо Аншуц и Универзитетот во Арканзас за медицински науки (UAMS)/Детскиот истражувачки институт во Арканзас (ACRI) опишува нов метод за дијагноза на LRTI кај деца со тешка респираторна инсуфициенција.
Методот го применува машинското учење на податоците за метагеномско секвенционирање добиени од белодробната течност на интубираните деца за да се дијагностицира педијатриски LRTI и да се идентификува нејзината причина со многу висока точност, што е далеку од сегашните техники.
LRTI може да биде предизвикана од широк спектар на бактериски, вирусни или габични патогени, но симптомите на инфекција изгледаат клинички слични без разлика на виновникот и дури тешко се разликуваат од неинфективните респираторни состојби. Поради ограничувањата на постојната дијагностика, лекарите често работат под „магла на војната“ кога станува збор за развој на ефективен план за лекување, рече Еран Мик, научник за биоинформатика во CZ Biohub SF и UCSF и еден од водечките автори на студијата.
Тековната дијагностика често се потпира на растечки бактерии од примероци од белодробна течност во културата, што одзема многу време и не секогаш правилно ги идентификува бактериските видови одговорни за проблемот. Тестовите често генерираат лажно-негативни резултати или откриваат случајни микроби кои всушност не предизвикуваат болест.
„Во повеќе од половина од сите случаи, вистинскиот микроб што ја предизвикува инфекцијата не е идентификуван“, рече соодветниот автор Чаз Ланџелиер, истражувач на CZ Biohub SF и вонреден професор по медицина во Одделот за заразни болести на UCSF. „Резултатите се дека дадените третмани не се нужно насочени кон она што го предизвикува проблемот“.
Наместо тоа, лекарите може да препишат коктел од антибиотици со широк спектар во обид да ја спречат сомнителната инфекција, што придонесува за појава на бактерии со отпорност на антибиотици. Оваа практика, исто така, може да доведе до негативни исходи на пациентот како повреда на бубрезите или инфекција од други штетни бактерии, како што е Clostridioides difficile. А може дури и да биде целосно неефективен против предизвикувачкиот патоген, како во случајот со вирусни инфекции.
„Додека вирусите предизвикуваат поголемиот дел од LRTI кај малите деца, знаеме дека децата со тешка LRTI на кои им е потребна механичка вентилациска поддршка често имаат истовремени инфекции на вирус и бактерии“, рече ко-виш автор Питер Мурани, професор по педијатрија во медицината за критична нега. во УАМС и претседател на АКРИ.
„Значи, дури и ако вирусот е откриен со вообичаено употребувано PCR тестирање, лекарите често се чувствуваат принудени да лекуваат можна бактериска инфекција, вклучително и кога клиничките култури се негативни. Повеќето деца добиваат антибиотици пред собирањето примероци што потоа може да придонесе за лажно-негативна култура резултати“.
„Дополнување на предизвиците со дијагностицирање на LRTI е тоа што вистинската биологија на инфекциите на долните дишни патишта не се однесува само на патоген микроб“, рече Лангелиер. „Тоа е навистина динамична интеракција помеѓу патогенот што ја предизвикува инфекцијата, имунолошкиот одговор на пациентот и нормалниот микробиом на белите дробови.
За подобро дијагностицирање и лекување на LRTI кај децата, истражувачите развија нов метод кој го зема предвид не само присуството на потенцијални патогени во белите дробови, туку и имунолошкиот одговор на пациентот, што може да покаже дали телото навистина се бори со инфекција.
Методот се потпира на метагеномско секвенционирање на РНК, кое истовремено известува за генската експресија на пациентот и за сите присутни микроби, сите од еден примерок од белодробна течност. Метагеномика ги доловува сите генетски секвенци присутни во примерокот – без разлика дали од пациентот, бактериите или вирусите. Тие секвенци потоа може пресметковно да се споредат со референтни бази на податоци за да се измери генската експресија и изобилството на микроби.
Истражувачите потоа примениле алгоритми за машинско учење на метагеномските податоци за да ги идентификуваат заедничките обрасци на генска експресија и изобилството на микроби кои го разликуваат вистинскиот LRTI од непоштетното присуство на микроби кои се инхерентен дел од белодробниот микробиом.
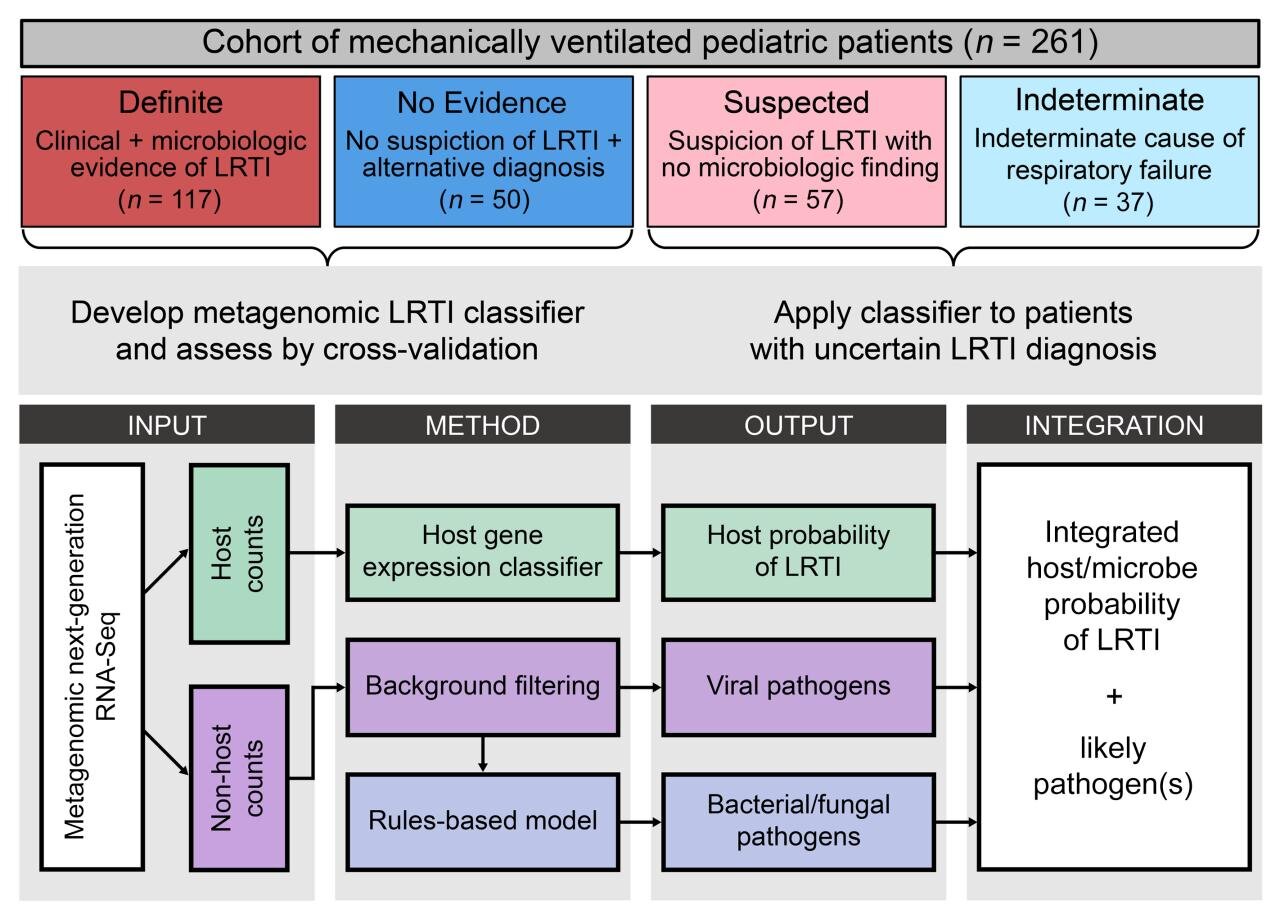
Истражувачите генерирале и проучувале метагеномски податоци од група од 261 дете со акутна респираторна инсуфициенција кои биле примени во една од осумте детски болници во САД за правилно да ги обучат алгоритмите за машинско учење, тим од лекари ригорозно пресуди дали секое од децата има LRTI, јасна неинфективна причина за респираторна инсуфициенција или несигурна дијагноза.
Податоците од пациенти окарактеризирани како дефинитивно кои страдаат од LRTI и од пациенти кои немаат докази за LRTI беа користени за да се развие и потоа да се тестира метагеномската дијагностика. Покрај поставувањето дијагноза, методот го номинира и најверојатниот причински патоген за пациентите кои се класифицирани како инфицирани.
Методот се покажа како неверојатно точен. „Работеше подобро од очекуваното“, рече Ланжелие. „Нашата „површина под кривата“, која во суштина е мерка за перформансите на дијагностички тестови, беше над 0,98, на скала од 0 до 1. Тоа е приближно толку добро колку што може да се постигне со дијагностички тест и всушност е подобро од сличен тест што го развивме кај возрасни“.
Концептот за оваа работа произлезе од претходното истражување на Лангелиер, Катрина Калантар од иницијативата Чан Цукерберг (CZI), професорот на UCSF и претседателот на SF Biohub Џо ДеРиси и нивните колеги, во кои тие користеа метагеномика за ефикасно дијагностицирање на инфекции на долниот респираторен тракт во критична болни возрасни пациенти.
Дијагностика за 21 век
„Овој тест би имал големо клиничко влијание“, рече Александра Цициклис, водечки автор на студијата и поранешен член на лабораторијата на Ланџелиер сега во Имунаи со седиште во Њујорк. „Една од клучните предности на метагеномската дијагностика е способноста да се даде одговор кај пациентите со несигурна клиничка дијагноза. Навистина, методот можеше да дијагностицира LRTI и да ги идентификува веројатните патогени за многу од пациентите кои не спаѓаат во една од двете дефинитивни категории на клиничка дијагноза што се користат за обука на моделот за машинско учење.
Покрај тоа, рече Цициклис, тест како овој може да се користи за да се исклучи бактериска инфекција, така што антибиотиците би можеле да се избегнат конкретно за овие пациенти, додавајќи: „Ова е еден од следните чекори што ќе го направат уште покорисен клинички. ”
Истражувачите се надеваат дека по понатамошна валидација, нивниот дијагностички метод ќе стане вообичаен во болничките услови. „Начинот на кој функционира дијагнозата за заразни болести е многу примитивен. Тоа е исто како што беше со децении и лекарите не се задоволни со алатките што ги имаат. Затоа се надеваме дека ова е нешто на што можеме да продолжиме да работиме за да дојдеме до точка каде што се спроведува во болница“, изјави Мик. „Се обидуваме да ја поставиме сцената за доведување на болниците во 21 век.
Повеќе информации:
Еран Мик и сор., Интегрираната метагеномика на домаќин/микроби овозможува точна дијагноза на инфекција на долниот респираторен тракт кај критично болните деца, Журнал за клиничко истражување (2023). DOI: 10.1172/JCI165904.