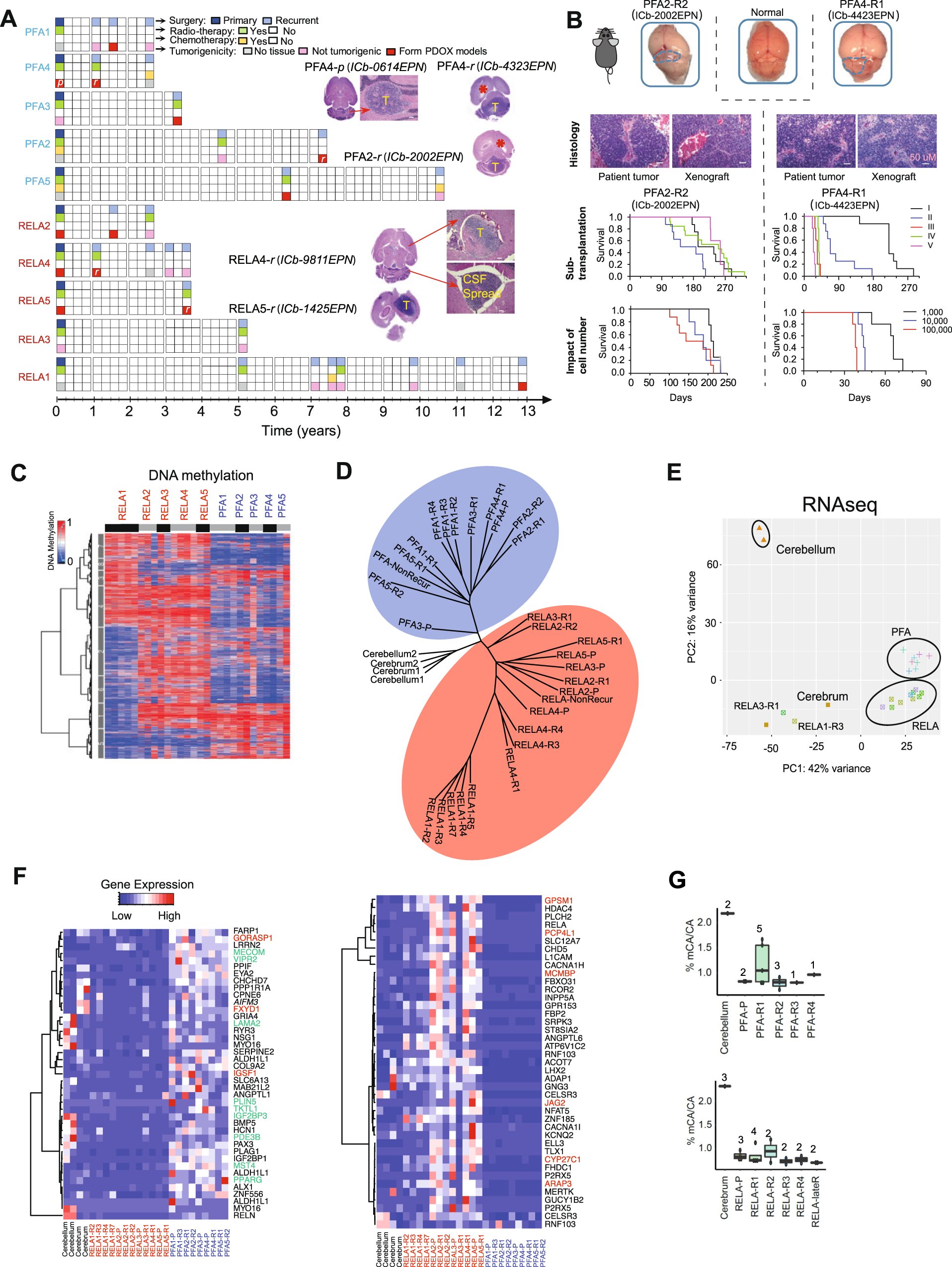
Истражувачите идентификуваа претходно непознати групи на епигенетски промени кај педијатриските тумори на мозокот, кои би можеле да послужат како нови терапевтски цели и да обезбедат алтернативни опции за третман за пациентите, според студијата на Northwestern Medicine објавена во Nature Communications.Ксиао-Нан Ли, д-р, д-р, Рејчел и Марк Гордон, професор по истражување на ракот и член на сеопфатниот центар за рак Роберт Х. Лури на Универзитетот Нортвестерн, беше постар автор на студијата.
Педијатрискиот епендимом, третиот најчест тип на рак на мозокот кај децата, моментално има стапка на повторување од 50% и повеќето пациенти на крајот ќе подлегнат на болеста поради слабиот одговор на третманот.
Додека ракот е агресивен и повторувањето е вообичаено, туморите растат побавно во споредба со другите типови на тумори на мозокот, нудејќи им мал прозорец за тимовите за нега на пациенти да пробаат различни стратегии за третман, вклучително и ресекција на повторливи тумори. Иако операцијата и зрачењето можат да помогнат во продолжување на преживувањето на пациентот, итно се потребни поефикасни и долгорочни опции за третман, според Ли.
Во тековната студија, тимот на Ли изврши секвенционирање на метилација на ДНК заедно со секвенционирање на РНК за да се идентификуваат епигенетските промени со користење на примероци од примарно и рекурентно ткиво на тумор на епендиом од 10 педијатриски пациенти кои биле третирани со зрачење и доживеале повторување на ракот повеќе пати во текот на 13- годишен период.
Од овој уникатен сет на тумори на пациенти, истражувачите развија нов панел од модели на ортотопски ксенографти глувци добиени од пациенти, кои се критички потребни за подобрување на разбирањето на биологијата на туморот и за тестирање на нови терапии, според Ли.
„Епендимомот е многу интересен тумор, и за разлика од многу други човечки канцери, мутациите не се главна причина. Кај овој тумор, мутациите ги нарекуваме „тивки“ бидејќи нема многу мутации. Промените се главно на страната на епигенетиката. , и затоа се фокусираме на метилација на ДНК“, рече Ли, кој исто така е професор по педијатрија во Одделот за хематологија, онкологија и трансплантација на матични клетки.
Користејќи ги моделите на ксенографт, истражувачите идентификуваа три уникатни групи на епигенетски мутации.
Првиот сет вклучуваше диференцијално изразени гени кои беа регулирани со потенцијални „двигатели“ области на метилација на ДНК (DMRs), или геномски региони кои содржат различни обрасци на метилација на ДНК, кои се пренесуваат од примарните тумори до туморите кои се повторуваат.
Вториот сет содржеше диференцијално изразени гени кои беа регулирани со потенцијални „засилувачи“ DMR, кои беа пронајдени само кај повторливи тумори. Конкретно, истражувачите открија дека генот PLEKHG1 е изразен во сите модели на рекурентни тумори што, според Ли, сугерира дека овој ген може да биде потенцијална терапевтска цел.
Третиот сет на мутации идентификувани кај примарните тумори беа „предвидувачи на релапс“ или збир на епигенетски маркери кои би можеле да помогнат да се предвиди дали туморот има висок ризик од повторување. Овие предвидувачи би можеле да им помогнат на давателите на услуги да избегнат непотребен третман на пациентите што може да доведе до дополнителни компликации по патот, според Ли.
„Педијатрискиот мозок сè уште се развива, и ако ги третирате непотребно премногу грубо, тоа ќе го одложи развојот и ќе го намали квалитетот на животот. Ако постои било каков начин да го предвидиме и подобриме нивниот квалитет на живот, тоа е многу важно“, рече Ли.
Понатаму, скринингот на овие двигатели и засилувачи може да помогне да се утврдат потенцијалните терапевтски цели и прецизни стратегии за лекување базирани на лекови.
„Важните работи што треба да се знаат се дека рекурентните тумори и не се сосема исти како примарните тумори – тие многу се менуваат – и за овој тип на студии, потребна ни е поголема соработка. Треба да работиме со што е можно повеќе болници и институции. рече Ли.